Test de diagnóstico rápido de VIH falsificados que circulan en las regiones de la OMS de las Américas y África
Esta alerta de producto medico se refiere a un dispositivo médico de diagnóstico in vitro (IVD) del virus de inmunodeficiencia humana (VIH) confirmado como falsificado en circulación en Guyana y Kenia.
A través del Sistema de Vigilancia y Seguimiento (GSMS) de productos médicos de calidad
subestándar y falsificados, la OMS fue informada de la circulación de al menos 8240 test de diagnóstico rápido falsificados para la detección de VIH-1/2 en Guyana. El producto es Uni-Gold™ HIV y declara ser
fabricado por Trinity Biotech plc. Notificaciones posteriores revelan que el mismo producto se encuentra en circulación en Kenia.
Uni-Gold™ HIV es un test de diagnóstico rápido de un sólo uso; este inmunoensayo para la detección cuantitativa de anticuerpos VIH-1 y VIH-2 se realiza en suero, plasma y sangre completa. Uni-Gold™ HIV está diseñado para utilizarse en puntos de atención al paciente para el diagnóstico de infección por VIH-1 y VIH-2.
Las pruebas de estrategia de la OMS recomiendan tres pruebas reactivas de VIH para confirmar que un paciente es seropositivo. El uso del producto Uni-Gold™ HIV falsificado, asunto de la alerta sobre productos médicos n°2/2020, es susceptible de conducir a un diagnóstico tardío de seropositividad.
Tabla 1: Detalles específicos del producto falsificado Uni-Gold™ HIV, señalado en la alerta de la OMS sobre productos médicos n°2 de 2020
Nombre del producto | Uni-Gold™ HIV | Uni-Gold™ HIV |
| Código del producto | 1206502 | 1206502 |
Número de lote | HIV7120026 | HIV6120030 |
Fecha de caducidad | 5 DEC 2020 | 29 JUL 20 |
Fabricante declarado | Trinity Biotech | Trinity Biotech |
El embalaje de este kit de test de VIH falsificados está en inglés.
El auténtico fabricante (Trinity Biotech plc) ha confirmado que:
- Ellos no fabricaron los productos falsificados descritos en la tabla 1.
- Los lotes auténticos HIV7120026 y HIV6120030 fueron fabricados por Trinity Biotech plc y ambos caducaron en 2019.
- Las fechas de caducidad son falsificadas y no corresponden con el registro de fabricación de los lotes.
Las fotografías de los productos mencionados se encuentran disponibles en la página 2 y la recomendación al público en la página 3.
Fotografías de los test de diagnóstico rápido de VIH confirmados como falsificados encontrados en Guyana

Fotografía 2 - Producto Uni-Gold™ HIV falsificado con inconsistencias en el etiquetado.

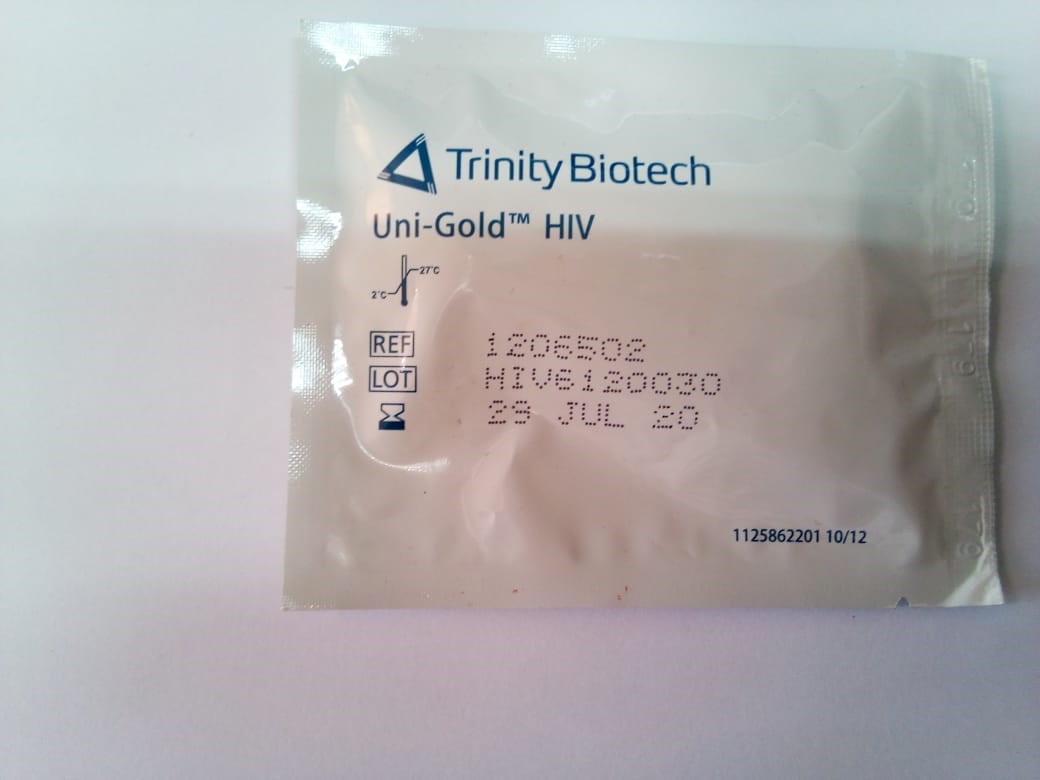
Fotografía 3 - Producto Uni-Gold™ HIV falsificado, lote HIV6120030, fecha de caducidad falsificada.
Consejos sobre las medidas que los usuarios deben tomar:
- Verifique la presencia de test Uni-Gold™ HIV con número de lote HIV7120026 o HIV6120030 en sus instalaciones.
- Si está en posesión de estos kits de pruebas falsificados con el número de lote HIV7120026 o HIV6120030:
- Por favor, no lo utilice.
- Comuníquese de inmediato con la organización que le suministró el producto (ya sea su programa de pruebas de VIH, organización no gubernamental o distribuidor local).
- Póngase en contacto con Trinity Biotech plc:
Teléfono: +353 1 276 9800
Correo electrónico: hiv@trinitybiotech.com
- Póngase en contacto con su autoridad sanitaria nacional.
Todos los productos médicos deben obtenerse a partir de fuentes auténticas y fiables. Su autenticidad y estado deben comprobarse de forma minuciosa.
Consejos sobre las medidas que deben tomar las autoridades sanitarias nacionales:
La OMS solicita un mayor escrutinio dentro de las cadenas de suministro de todos los países, particularmente en los lugares donde se realizan estos test (centros de salud, centros comunitarios), laboratorios clínicos, tiendas/almacenes médicos e instalaciones de los operadores económicos relevantes (agentes, representantes autorizados, distribuidores, mayoristas, etc.).
Si descubre estos test falsificados con número de lote HIV7120026 o HIV6120030, no los utilice.
Se ruega a las autoridades sanitarias nacionales que notifiquen inmediatamente a la OMS en caso de que detecten la presencia de estos productos falsificados en su país y utilicen el formulario de quejas de productos de diagnóstico in vitro de la OMS.
Si tiene usted alguna información acerca de la fabricación, la distribución o el suministro de estos productos, póngase en contacto con rapidalert@who.int.
Sistema OMS de Vigilancia y Seguimiento de
Productos Médicos de Calidad Subestándar y Falsificados
Para más información, diríjase a nuestros sitio web: https://www.who.int/medicines/regulation/ssffc/en/
