Hidroclorotiazida falsificada (que contiene glibenclamida) en el Camerún
Esta Alerta sobre Productos Médicos hace referencia a la circulación en la Región de África de la OMS de hidroclorotiazida cuya falsificación está confirmada y que contiene glibenclamida en vez de hidroclorotiazida. Se han notificado efectos adversos atribuidos a este producto. La hidroclorotiazida genuina se utiliza como antihipertensivo y diurético, mientras que la glibenclamida es un antidiabético.
En marzo de 2019 la OMS fue informada por una organización no gubernamental del Camerún de que un medicamento presentado como hidroclorotiazida 50 mg había producido hipoglucemia a los pacientes. Los análisis preliminares revelaron que el producto no contenía en absoluto el principio activo declarado, la hidroclorotiazida, y en vez de ello se identificó la presencia de glibenclamida. Tras verificación con el fabricante declarado, se confirmó que este producto es falsificado. Las autoridades locales fueron informadas del incidente.
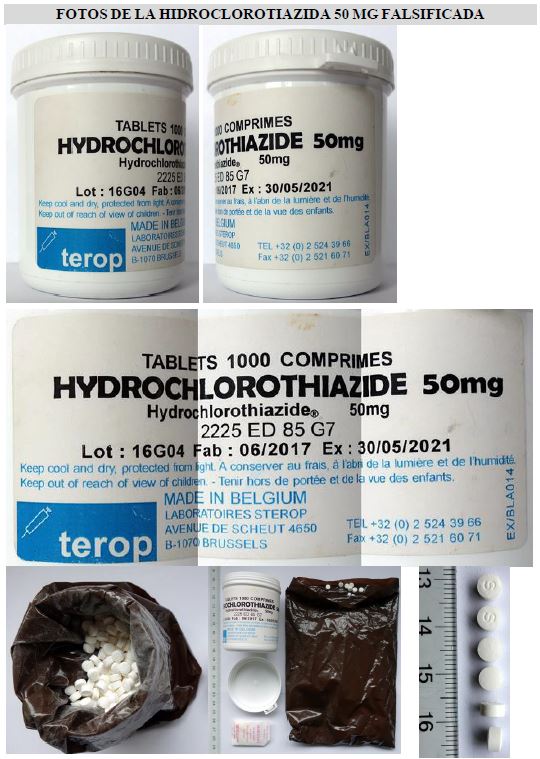
Cuadro 1: Datos del producto falsificado, hidroclorotiazida 50 mg, objeto de la Alerta N° 6/2019 de la OMS

El producto se presenta en envases de plástico con 1000 comprimidos, etiquetados en francés e inglés.
Ulteriores análisis de confirmación han establecido que el producto:
- no contiene en absoluto el principio activo esperado, la hidroclorotiazida, pero
- sí contiene aproximadamente 5 mg de glibenclamida
Esto supone un riesgo para los pacientes que estén tomando hidroclorotiazida para tratar la hipertensión. Nótese que ha habido casos de hipoglucemia en pacientes del Camerún que han sido atribuidos al uso de la mencionada “hidroclorotiazida” con número de lote 16G04.
En la etiqueta adherida a los envases de plástico de este producto se declara que el fabricante es Sterop. Sin embargo, la empresa ha confirmado a la OMS:
- que no fabricó ni suministró el producto y
- que el número de lote y otros detalles de la etiqueta no se corresponden con los registros de fabricación genuinos.
La OMS pide que se aumente la vigilancia en las cadenas de suministro de los países que pudieran verse afectados por este producto médico falsificado. Dicho aumento de la vigilancia debería incluir a los hospitales, clínicas, centros de salud, mayoristas, distribuidores, farmacias y cualquier otro proveedor de productos médicos.
Si está en posesión del producto mencionado, se le ruega que no lo utilice. Si lo ha utilizado o si presenta algún evento adverso tras su administración u observa una falta inesperada de eficacia, se le ruega que consulte de inmediato a un profesional sanitario cualificado y se asegure de que este notifica el incidente al Ministerio de Salud, a la Autoridad Nacional de Reglamentación de los Medicamentos o al Centro Nacional de Farmacovigilancia.
Todos los productos médicos deben obtenerse a partir de fuentes auténticas y fiables. Su autenticidad y estado deben comprobarse de forma minuciosa. En caso de duda, asesórese con un profesional sanitario.
Se ruega a las autoridades sanitarias nacionales que notifiquen inmediatamente a la OMS en caso de que detecten la presencia de este producto médico falsificado en su país. Si tiene alguna información acerca de la fabricación, distribución o suministro de este producto se le ruega que se ponga en contacto con rapidalert@who.int
WHO Global Surveillance and Monitoring Systemfor Substandard and Falsified Medical Products
For further information, please visit: http://www.who.int/medicines/regulation/ssffc/en/
