Apprenez-en plus à propos des vaccins, depuis leur fonctionnement jusqu’à leur fabrication, grâce à la série de l’OMS « Les vaccins expliqués ».
Comment les vaccins sont-ils développés et fabriqués ?
La mise au point d’un vaccin commence par un besoin en santé publique, qu’il s’agisse de prévenir une nouvelle maladie émergente ou d’améliorer les vaccins actuels. Le développement d’un vaccin se déroule en plusieurs phases, impliquant une étroite collaboration entre les chercheuses et chercheurs du monde universitaire, les institutions de santé publique, les organismes de réglementation et les entreprises pharmaceutiques.
Comme pour tous les médicaments, chaque vaccin doit faire l’objet de tests approfondis et rigoureux pour garantir son innocuité avant de pouvoir être introduit dans le programme de vaccination d’un pays. Les vaccins les plus couramment utilisés aujourd’hui sont employés depuis des décennies, et des millions de personnes les reçoivent en toute sécurité chaque année.
Phase préclinique
Chaque vaccin en cours de développement doit au préalable faire l’objet de tests et d’évaluations afin de déterminer quel antigène doit être utilisé pour déclencher une réponse immunitaire. Cette phase préclinique se fait sans test sur l’être humain. Un vaccin expérimental est d’abord testé sur des animaux afin d’évaluer son innocuité et son potentiel de prévention des maladies.
Si le vaccin déclenche une réponse immunitaire, il est alors testé dans le cadre d’essais cliniques sur l’être humain en trois phases.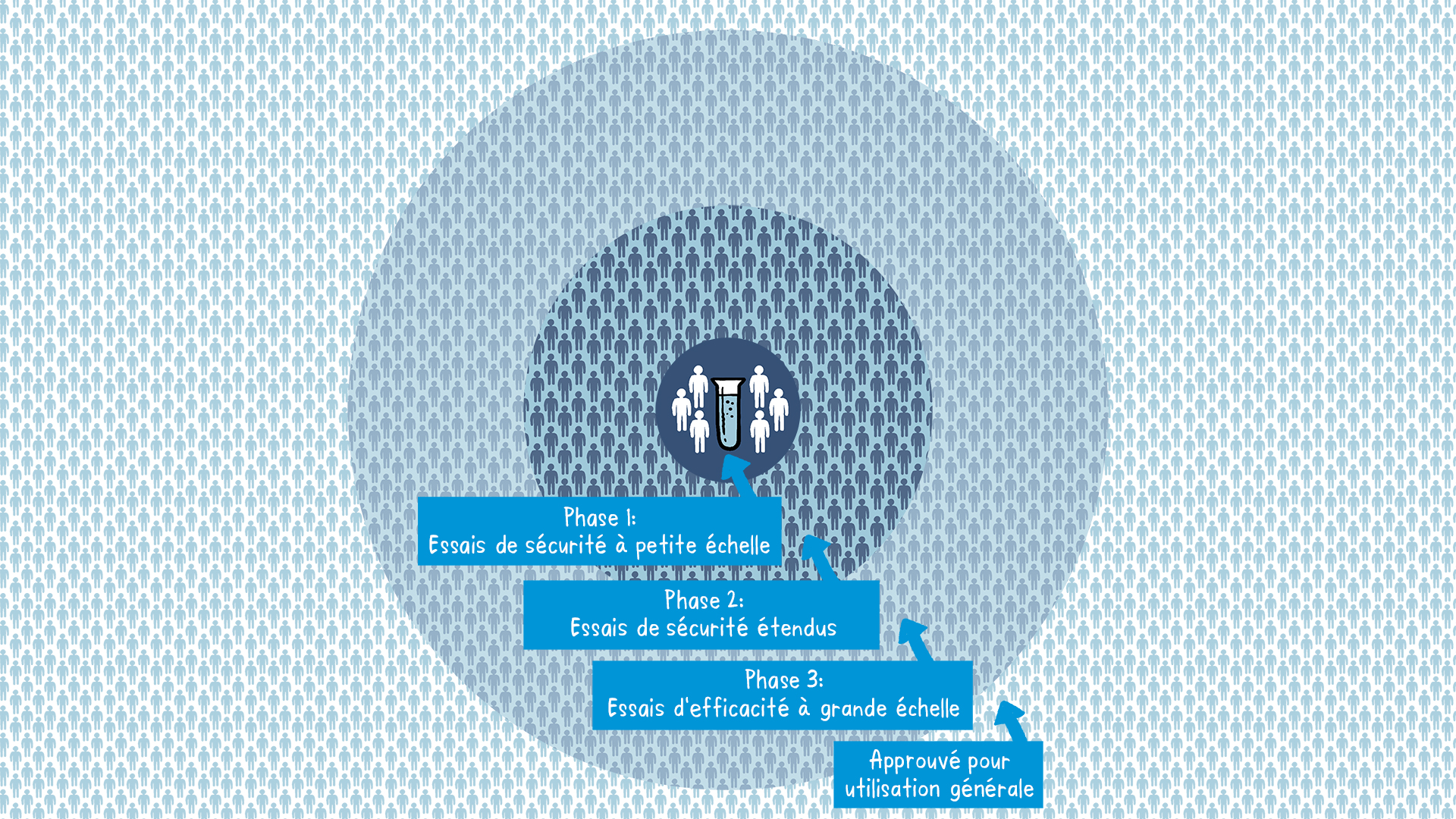
Phase 1
Le vaccin est administré à un nombre restreint de volontaires afin d’évaluer son innocuité, de confirmer qu’il provoque une réponse immunitaire et de déterminer le bon dosage. Généralement, au cours de cette phase, les vaccins sont testés sur de jeunes adultes volontaires en bonne santé.Phase 2
Le vaccin est ensuite administré à plusieurs centaines de volontaires afin d’évaluer de manière plus approfondie son innocuité et sa capacité à déclencher une réponse immunitaire. Les participantes et participants à cette phase présentent les mêmes caractéristiques (telles que l’âge, le sexe) que les personnes auxquelles le vaccin est destiné.
Cette phase comporte généralement plusieurs essais pour évaluer les différents groupes d’âge et les différentes formulations du vaccin. Un groupe qui n’a pas reçu le vaccin est généralement inclus dans la phase en tant que groupe comparatif afin de déterminer si les changements observés chez le groupe vacciné sont attribués au vaccin ou s’ils sont survenus par hasard.
Phase 3
Le vaccin est ensuite administré à des milliers de volontaires — et comparé à un groupe similaire de personnes qui n’ont pas reçu le vaccin, mais qui ont reçu un produit comparatif — afin de déterminer si le vaccin est efficace contre la maladie contre laquelle il est conçu et d’étudier son innocuité chez un groupe de personnes beaucoup plus important.
La plupart du temps, les essais de phase 3 sont réalisés dans plusieurs pays et sur plusieurs sites dans un même pays afin de garantir que les résultats des performances du vaccin s’appliquent à plusieurs populations différentes.
Au cours des phases deux et trois des essais, les volontaires et les scientifiques qui mènent l’étude ignorent quels sont les volontaires qui ont reçu le vaccin testé ou le produit comparatif. Cette méthode en aveugle est nécessaire pour garantir que ni les volontaires ni les scientifiques ne soient influencés dans leur évaluation quant à l’innocuité ou l’efficacité du fait de leur connaissance de l’identité des personnes ayant reçu le produit.
Une fois l’essai conclu et tous les résultats finalisés, les volontaires et les scientifiques ayant participé à l’essai sont informés des personnes qui ont reçu le vaccin et de celles qui ont reçu le produit comparatif.
Lorsque les résultats de l’ensemble de ces essais cliniques sont disponibles, une série d’étapes est nécessaire, notamment l’examen de l’efficacité et de I’innocuité en vue de l’approbation au regard des politiques réglementaires et de santé publique. Les responsables de chaque pays examinent attentivement les données de l’étude et décident d’autoriser ou non l’utilisation du vaccin.
Comment un vaccin est-il approuvé aux fins de la fabrication ?
Une fois les essais cliniques terminés, un vaccin doit être évalué par l’organisme de réglementation compétent pour s’assurer qu’il répond à des normes strictes en matière de qualité, d’innocuité et d’efficacité. Une fois le vaccin approuvé, les fabricants peuvent le soumettre à l’OMS à des fins de préqualification, un processus d’évaluation qui permet d’assurer qu’il répond aux normes mondiales.
En cas d’urgence sanitaire mondiale, comme en cas de pandémie, le protocole OMS d’autorisation d’utilisation d’urgence (EUL) peut être utilisé pour accélérer l’accès aux vaccins essentiels tout en maintenant des contrôles de sécurité rigoureux. Ce processus accéléré mais exhaustif permet de s’assurer que les vaccins parviennent aux personnes qui en ont besoin le plus rapidement possible, dans un délai limité et en fonction d’une évaluation des risques par rapport aux avantages.
Le processus de préqualification suivant le protocole EUL de l’OMS aide l’ONU et d’autres organisations internationales d’approvisionnement à déterminer si le vaccin peut être utilisé par les programmes de vaccination.
Vaccins contre la COVID-19 : comment le développement a-t-il été accéléré ?
En règle générale, les entreprises travaillent de manière indépendante pour mener à bien les projets de développement clinique d’un vaccin. Une fois qu’un vaccin est autorisé, la fabrication commence à monter en puissance. Le processus, des essais précliniques à la fabrication, peut prendre plus d’une décennie.
Cependant, dans des situations urgentes comme la pandémie de COVID-19, le développement de vaccins peut être accéléré sans compromettre la qualité et la sécurité. Pour les vaccins contre la COVID-19, les spécialistes de la recherche et de la conception de vaccins ont travaillé en parallèle sur plusieurs phases différentes, soutenus par des engagements financiers et politiques sans précédent. Cela a permis un développement plus rapide tout en maintenant une surveillance réglementaire rigoureuse.
Comment les vaccins sont-ils emballés ?
Une fois que le vaccin a été fabriqué en grande quantité, il est conditionné dans des flacons en verre, des seringues ou des ampoules préremplies, puis emballé soigneusement pour un stockage au froid et un transport en toute sécurité.
L’emballage des vaccins doit pouvoir résister à des températures extrêmes, ainsi qu’aux risques liés au transport à l’échelle mondiale. Par conséquent, les flacons de vaccin sont le plus souvent en verre, s’agissant d’un matériau durable et capable de maintenir son intégrité dans des températures extrêmes.
Comment les vaccins sont-ils stockés ?
Lorsqu’un vaccin est trop chaud ou trop froid, il devient moins efficace, voire inactif. S’ils ne sont pas stockés à la bonne température, les vaccins peuvent être détériorés ou dangereux à utiliser. La plupart des vaccins nécessitent un stockage réfrigéré entre 2 et 8 °C. D’autres ont besoin de températures pouvant aller jusqu’à -20 °C. Certains des vaccins les plus nouveaux doivent être conservés ultrafroids à -80 °C. Pour ce qui concerne les vaccins congelés, certains d’entre eux peuvent être stockés en toute sécurité entre 2 et 8 °C pendant une période limitée.
Les réfrigérateurs ordinaires ne peuvent pas maintenir une température uniforme et constante, aussi des réfrigérateurs médicaux spécialisés doivent être utilisés pour ces précieux produits et leur température est régulièrement ou constamment contrôlée.
Comment les vaccins sont-ils expédiés ?
Pour maintenir cette chaîne du froid, les vaccins sont expédiés à l’aide d’équipement spécifique qui ne compromet pas l’intégrité du produit. Une fois que les expéditions arrivent dans le pays de destination, des camions réfrigérés transportent les vaccins de l’aéroport à la chambre froide de l’entrepôt. De là, des glacières portatives sont utilisées pour transporter les vaccins de la chambre froide vers les centres régionaux où ils sont stockés dans des réfrigérateurs. Si la vaccination a lieu à l’extérieur de l’établissement régional, la dernière étape nécessite souvent des glacières portatives pour transporter les produits vers les sites réservés aux campagnes de vaccination.
Les nouvelles technologies ont permis de mettre au point des dispositifs portables qui peuvent maintenir les vaccins à la température froide voulue pendant plusieurs jours sans avoir besoin d’électricité.
Contrôle de la qualité
Il faut prouver l’innocuité et l’efficacité d’un vaccin sur une large population avant qu’il ne soit approuvé et introduit systématiquement dans un programme national de vaccination. Les critères d’innocuité et d’efficacité des vaccins sont extrêmement élevés, car les vaccins sont administrés à des personnes qui sont en bonne santé et qui ne souffrent pas de la maladie.
Un suivi supplémentaire est effectué de manière continue après l’introduction du vaccin. Il existe des systèmes permettant de surveiller l’innocuité et l’efficacité de tous les vaccins. Cela permet aux scientifiques de suivre l’impact et l’innocuité des vaccins y compris lorsqu’ils sont utilisés chez un grand nombre de personnes, sur une longue période. Ces données sont utilisées pour ajuster les politiques d’utilisation des vaccins afin d’optimiser leur impact, et elles permettent également de suivre le vaccin en toute sécurité tout au long de son utilisation.
Une fois qu’un vaccin est utilisé, il doit faire l’objet d’un suivi continu pour s’assurer que son innocuité persiste.
Une fois que les vaccins commencent à être administrés, les autorités nationales et l’OMS surveillent en permanence les effets secondaires indésirables possibles — et en déterminent la gravité — ainsi que les réponses des personnes qui ont été vaccinées. L’innocuité du vaccin est primordiale, avec des évaluations régulières et des études cliniques post-homologation pour rendre compte de son innocuité et de son efficacité.
Des études sont souvent menées pour déterminer combien de temps un vaccin donné reste protecteur.
