Ampoules d'antimoniate de méglumine falsifiées en Iran et au Pakistan
Cette alerte produit médical concerne deux produits falsifiés circulant en Iran et au Pakistan, contenant prétendument de l'antimoniate de méglumine pour le traitement de la leishmaniose. Ces deux produits falsifiés sont présentés dans des ampoules en verre transparent et le fabricant mentionné sur l'emballage est Tillotts Pharma AG. La circulation de ces produits médicaux falsifiés est confirmée dans la Région OMS de la Méditerranée orientale.
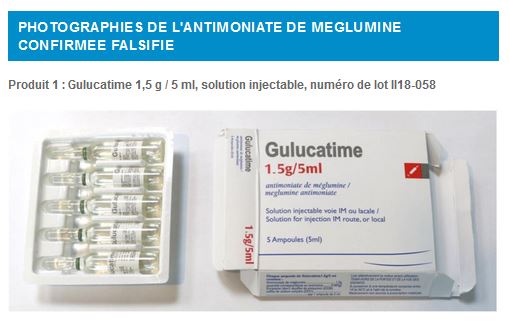
Falsified product n°1: GULUCATIME En janvier 2019, l'OMS a été informée qu'un produit appelé GULUCATIME était disponible au niveau des patients en Iran. Ce produit est prétendument fabriqué par Tillotts Pharma AG ; la vérification effectuée par l'OMS a confirmé que ce produit était falsifié. Il est présenté dans des emballages en carton contenant chacun cinq ampoules. L'emballage est en langue anglaise et en langue française, mais présente des fautes d'orthographe dans les deux langues. Les informations concernant ce produit sont présentées dans le Tableau 1 ci-dessous.
Produit falsifié n°2 : GULUCATIME. En mars 2019, l'OMS a été informée qu'un produit similaire appelé GLUCANTIME était disponible au niveau des patients au Pakistan. Ce produit est aussi prétendument fabriqué par Tillotts Pharma AG et est confirmé falsifié. Les photographies disponibles suggèrent que l'étiquette du produit est en langue anglaise seulement. Les informations concernant ce produit sont présentées dans le Tableau 1 ci-dessous.
Tableau 1 : Informations sur les produits GULUCATIME et GLUCANTIME falsifiés et objets de l'alerte produit médical N°7/2019 de l'OMS

Les résultats des analyses de laboratoire effectuées avec l'appui de l'OMS indiquent que le produit GULUCATIME n'a pas été fabriqué conformément aux bonnes pratiques de fabrication.
L'analyse en laboratoire du produit GLUCANTIME est en cours. Cette alerte produit médical N°7/2019 sera mise à jour et publiée sur le site Web de l'OMS dès que les résultats seront connus.
Aucune manifestation indésirable connue, attribuée à l'utilisation de l'un ou l'autre des deux produits falsifiés mentionnés ci-dessus, n'a été signalée à l'OMS à ce stade.
L'emballage ou les étiquettes des deux produits référencés ci-dessus (Gulucatime et Glucantime) indiquent "fabriqué pour Tillotts Pharma AG ". Toutefois, la société Tillotts Pharma AG a confirmé à l'OMS que elle ne fabrique pas, ne sous-traite pas la fabrication et ne distribue pas ces produits nulle part dans le monde.

L’OMS demande une vigilance accrue au niveau des chaînes d’approvisionnement dans les pays susceptibles d'être concernés par ces produits médicaux falsifiés. Cette vigilance renforcée s'applique aux hôpitaux, dispensaires, centres de santé, grossistes, distributeurs, pharmacies et à tout autre fournisseur de produits médicaux.
Si vous êtes en possession de ces produits, veuillez ne pas les utiliser. Si toutefois vous avez pris ces produits médicaux falsifiés ou si vous souffrez de manifestations indésirables ou d'un manque d'efficacité inattendu, veuillez consultez immédiatement un professionnel de la santé qualifié et vous assurer qu'il notifie cet incident au Ministère de la santé, à l'Autorité nationale de réglementation du médicament ou au Centre national de pharmacovigilance.
Tout produit médical doit être obtenu auprès de sources authentiques et fiables. L’authenticité et l’état du produit doivent être soigneusement vérifiés. En cas de doute, demandez conseil à un professionnel de la santé.
Les autorités sanitaires nationales sont priées d'informer immédiatement l’OMS si ces produits médicaux falsifiés sont découverts dans leur pays. Si vous avez des informations concernant la fabrication, la distribution ou la circulation de ces produits médicaux, veuillez écrire à rapidalert@who.int
WHO Global Surveillance and Monitoring Systemfor Substandard and Falsified Medical Products
For further information, please visit: http://www.who.int/medicines/regulation/ssffc/en/
