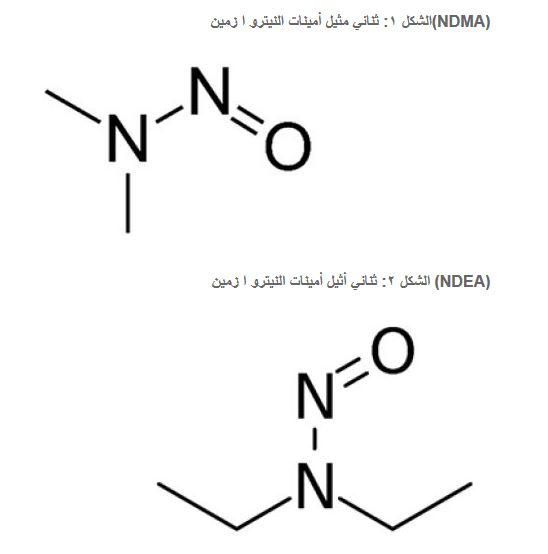
معلومات أساسية
علمت سلطات تنظيم الأدوية بتموز/ يوليو ٢٠١٨ لأول مرة بوجود شوائب النيترو ا زمينات من ثنائي مثيل أمينات النيترو ا زمين في المنتجات الطبية الحاوية على مادة الفالسارتان. وهذه المادة هي عبارة عن عامل مثبط لاستقبال هرمون (NDMA) الأنجيوتنسين المتحول في صيغته الثانية، وهي تنتمي إلى سلالة المركبات المتناظرة والمُ شار إليها عادةً باسم مركبات السارتان.
وكُشف لاحقاً عن وجود المزيد من شوائب النيترو ا زمينات بأدوية أخرى تنتمي إلى سلالة مركبات السارتان، بما فيها ثنائي (NEIPA) وأثيل إيزوبروبيل أمينات النيترو ا زمين (NDIPA) وإيزوبروبيل أمينات النيترو ا زمين (NDEA) أثيل أمينات النيترو ا زمين .(NMBA) وحمض مثيل رباعي أمينوبوتيريك النيترو ا زمين
وأبلغ بالآونة الأخيرة عن وجود شوائب النيترو ا زمينات بالمنتجات الطبية الحاوية على مادتي البي وغليتازون وال ا رنيتيدين. ٣،١
ما هي النيتر و ا زمينات؟
على نحو أدق، إلى جميع الجزيئات الحاوية على الزم رة (N-nitrosoamines) يشير تعبير النيتر و ا زمين أو النيترو ا زمينات الوظيفية من المركبات النيتروزوية، وهي جزيئات تثير الانشغال لأن شوائب النيترو ا زمينات هي من المواد التي يُحتمل أن تكون مواد مسرطنة للإنسان. ورغم وجود هذه الشوائب أيضاً في بعض الأطعمة وإمدادات مياه الشرب، فإن وجودها بالأدوية يعتبر غير مقبول كذلك.
ما أسباب وجود النيترو ا زمينات؟
من المتعذر عموماً تكوين النيترو ا زمينات ما لم تتفاعل الأمينات الثانوية أو الثلاثية مع حمض النيتروز الذي هو حمض غير مستقر في حد ذاته، وإن تسنى تكوينه في الموقع من مركبات النتريت في ظل ظروف تحضير المركبات الحمضية.
أمّا في حالة مركبات السارتان، فإنها تحتوي في معظمها على حلقة التت ا رزول التي تُستعمل لتشكيلها مادة نيتريت الصوديوم. وتشاء الصدفة أن تكون المذيبات المستعملة في التشكيل هي إما مركبات الأمينات أو مركبات حاوية على مخلفات الأمينات، والتي يُرجح أن تتسبب في الملاحظ من شوائب ثنائي مثيل أمينات النيترو ا زمين وثنائي أثيل أمينات النيترو ا زمين في المنتجات، علماً بأن مصدر وجود شوائب ثنائي مثيل أمينات النيترو ا زمين في دفعات منتج ا رنيتيدين ما ا زل غامضاً حالياً.
ولكن خُ لِص أيضاً أثناء التحقيقات الجارية إلى أن احتمال احتواء المنتجات على شوائب النيترو ا زمينات هو أوسع نطاقاً من وجودها المت ا زمن، لا غير، في مركبات النيتريت والأمينات في توليفة المكونات الفعالة للمستحض ا رت الصيدلانية. ٤
وتشير البينات إلى أن مصادر مركبات النتريت أو الأمينات بوصفها ملوثات غير مقصودة للمواد الأولية والكواشف والمذيبات - مثل ثنائي مثيل الأمينات الموجود في الفورماميد الثنائي المثيل الشائع الاستعمال كمذيب - قد تهيئ أيضاً ظروفاً مواتية لتكوين النيترو ا زمينات التي قد تُتاح أيضاً فرص تكوينها بفعل انتقال مركبات النتريت أو الأمينات من خطوات التكوين اللاحقة. ومن الجدير بالذكر تحديد التلوث الخارجي المصادر بوصفه مصد ا رً لاحتواء المنتجات على النيترو ا زمينات، وخصوصاً منه التلوث الناجم عن استعمال المواد المعاد تدويرها والمذيبات الحاوية فعلاً على كميات من النيترو ا زمينات. ومن الأمثلة المستشهد بها على ذلك استعمال مادة الفورماميد الثنائي المثيل المعاد تدويرها التي تُخمّد بواسطة مركب نيتريت الصوديوم للتخلص من بقايا مادة الأزيد في إطار عملية الاسترداد. وعلاوة على ذلك، فإنه غالباً ما تُسند مهمة إعادة تدوير المواد والمذيبات إلى أط ا رف خارجية ثالثة قد لا تطبق ما يلزم من ضوابط في ضوء ما تحتويه المواد التي تجه زها من مركبات. ويمكن أن تصبح المواد والمذيبات ملوثة بالتبادل بالنيترو ا زمينات أو الشوائب التي قد تتفاعل بالمرحلة السفلى من إنتاجها لتكوين النيترو ا زمينات، إذا لم تُنظف كما ينبغي المعدات المتداولة بين العملاء. ٤ب
والأهم من ذلك أن هذه الآليات الإضافية، ولاسيما التلوث المتبادل، لا تلحق بمنتجات بعينها تحديداً إلى حد ما، وقد تؤثر على منتجات لا يُتوقع بخلاف ذلك أن تكون معرضة لخطر تكوين النيترو ا زمينات فيها. وقد دفعت هذه الشواغل الأوسع نطاقاً وكالة الأدوية الأوروبية ٥ إلى مطالبة جميع حملة ت ا رخيص تسويق منتجات المستحض ا رت الصيدلانية النهائية كافّة بإج ا رء تقييم لمخاط رها للبت في خطورة ما تحتويه من نيترو ا زمينات.
درجة السمية
تندرج مركبات ثنائي مثيل أمينات النيترو ا زمين وثنائي أثيل أمينات النيترو ا زمين ضمن نطاق الزم رة المسماة باسم "زم رة المواد المثيرة للانشغال"، وهي عبارة عن مجموعة من المواد المسرطنة والقادرة بشدة على التسبب في الطف ا رت والتي صنفتها الوكالة الدولية لبحوث السرطان التابعة للمنظمة على أنها مواد يُحتمل أن تكون مواد مسرطنة للإنسان. ورغم قوة شوائب النيترو ا زميناتات هذه، فإن خطورة تسبب الكميات الملحوظة منها في إصابة الإنسان بالسرطان ما فتأت جدّ متدنية.
ولا تتوفر سوى بيانات محدودة عن مدى سمية هذه الشوائب الموجودة تحديداً في مركبات ثنائي مثيل أمينات النيترو ا زمين وثنائي أثيل أمينات النيترو ا زمين. وبناءً على هذه المعلومات، فقد اعتمدت معظم الهيئات التنظيمية الرئيسية الكميات المقبولة مؤقتاً من مدخول هذه الشوائب المحددة على النحو المبين في الجدول ١ أدناه.
(NEIPA) وأثيل إيزوبروبيل أمينات النيترو ا زمين (NDIPA) ونظ ا رً إلى تشابه هياكل مركبات إيزوبروبيل أمينات النيترو ا زمين فإن الهيئات التنظيمية الدولية تنظر إلى مرتسم سميتها على أنه ،(NMBA) وحمض مثيل رباعي أمينوبوتيريك النيترو ا زمين مماثل لسمية مركبات ثنائي مثيل أمينات النيترو ا زمين وثنائي أثيل أمينات النيترو ا زمين.
3 وفيما يخص شوائب النيترو ا زمينات غير المدرجة في الجدول ١، فإنه يُوصى بتطبيق المبادئ المبينة بإيجاز في المبدأ ٨ لغرض تحديد المدخول المقبول منها، علماً بأن واحداً على الأقل من النيتر و ا زمينات المتناظرة ICH's M7(R التوجيهي ( 1 والداخلة في محتوى مركبات السارتان أثبت سلبيته لاختبار أميز. ٤
الإج ا رءات التنظيمية
طُلِب بالاتحاد الأوروبي عقب إج ا رء استع ا رض بموجب المادة ٣١ لمركبات السارتان المعرضة لخطر احتوائها على شوائب النيترو ا زمينات (الحاوية منها على حلقة التت ا رزول)، ٩ من الشركات المصنعة أن تستعرض إج ا رءاتها في مجال التصنيع وتدخل عليها ما يلزم من تعديلات للتقليل إلى أدنى حد من شوائب النيترو ا زمينات بأقصى قدر عملي ممكن. وأتيحت أمام تلك الشركات فترة انتقالية مدتها سنتان لإدخال تلك التعديلات، ويتواصل خلالها تطبيق المبين في الجدول ١ من حدود مس موح بها مؤقتاً من مدخول المنتجات. ولا يُسمح بالاتحاد الأوروبي بتداول دفعات المنتجات التي تتجاوز هذه الحدود فيما يخص ف ا ردى الشوائب، أو الدفعات الحاوية منها على كل من مركبات ثنائي مثيل أمينات النيترو ا زمين وثنائي أثيل أمينات النيترو ا زمين.
و يواظَ ب على إدخال التنقيحات اللازمة على دستور الأدوية الأوروبي فيما يخص الد ا رسات الإف ا ردية المتعلقة بالمواد الدوائية التي تحتويها سلسلة مركبات السارتان لكي تشمل اختبا ا رت الكشف عن النيتر و ا زمينات. وإضافة إلى ذلك، يجري على قدم وساق تنقيح الد ا رسة الإف ا ردية العامة المتعلقة بالمكونات الفعالة للمستحض ا رت الصيدلانية (الد ا رسة الإف ا ردية العامة رقم ٢٠٣٤ )، وستُدرج فيها أيضاً الاختبا ا رت المناسبة.
وبناءً على هذه التدابير المتخذة، فقد سُحبت مؤقتاً منتجات عديدة لمركبات السارتان من أسواق الاتحاد الأوروبي، وأُعيد الآن الكثير منها إلى أسواقه؛ ولكن الاتحاد الأوروبي ينصح المرضى بعدم وقف تناولهم لعلاجاتهم ما لم ينصحهم بذلك الصيدلاني أو الطبيب المعني بهم.
مدخول شوائب النيترو ا زمينات فيها، وفي سحب تلك الأدوية من الأس واق. وتنشر هذه الإدارة قائمة بأسماء منتجات الأدوية المثبطة لاستقبال هرمون الأنجيوتنسين المتحول في صيغته الثانية وحالة تلك المنتجات من حيث محت واها من النيتر و ا زمينات. ١٠ وشددت الإدارة المذكو رة شأنها شأن وكالة الأدوية الأوروبية، على أن مخاطر وقف تناول هذه الأدوية فجأة (مثل التعرض للسكتة الدماغية) تفوق بكثير المخاطر القليلة الناجمة عن مواصلة تناول هذه الأدوية الحاوية على تلك الشوائب.
وكُ شف بالآونة الأخيرة عن وجود كميات من شوائب ثنائي مثيل أمينات النيترو ا زمين في دفعات من منتجات ال ا رنيتيدين والني ا زتيدين، علماً بأن أدوية ال ا رنيتيدين تستعمل على نطاق واسع لتقليل إف ا رز عصا ا رت المعدة الحمضية لدى المرضى المصابين بحالات، مثل حرقة المعدة وقرحتها، وهي أدوية متاحة في الأسواق وتُصرف بدون وصفة طبية. 4 وتباينت ردود فعل الوكالات التنظيمية، واتخذ بعض الهيئات التنظيمية الوطنية الأوروبية، كل على حدة، وكذلك وكالة للمنتجات الطبية وو ا زرة الصحة الكندية، تدابير احت ا رزية قضت بسحب جميع منتجات ال ا رنيتيدين (Swissmedic) سويسميديك من الأسواق أو بوقف توزيعها حتى يثبت تحليل الوجبات الموزعة منها أن محتواها من ثنائي مثيل أمينات النيترو ا زمين هو دون المستويات المقبولة. و تُجري حالياً وكالة الأدوية الأور وبية تقييماً للبيانات المتاحة للبت فيما إذا كان المرضى الذين يستعملون دواء ال ا رنيتيدين معرضون لأي خطورة ناجمة عن ثنائي مثيل أمينات النيترو ا زمين. ١١
وطلبت سلطات أخرى، مثل إدارة الأدوية والأغذية بالولايات المتحدة، ألا تُسحب المنتجات طوعاً إلا إذا أثبتت نتائج اختبا رها أن مستويات ما تحتويه من مركبات ثنائي مثيل أمينات النيترو ا زمين هي أعلى من المستويات المحددة مؤقتاً، ١٢ وقررت تلك الإدارة أن مستويات هذه المركبات الملحوظة في معظم منتجات ال ا رنيتيدين والني ا زتيدين مماثلة لمستوياتها المتوقع وجودها في ما يتناوله المرء من أطعمة شائعة مثل اللحوم المشوية أو المدخنة.
وشرعت شركات كثيرة في اتخاذ تدابير وقائية تمثلت في سحب منتجاتها من ال ا رنيتيدين طوعاً من الأسواق.
أما وكالة الأدوية الأوروبية فقد اتخذت تدبي ا رً عاماً طلبت فيه من حملة ت ا رخيص تسويق منتجات المستحض ا رت الصيدلانية النهائية كافّة إج ا رء تقييم لإمكانية وجود النيتر و ا زمينات في جميع المنتجات الحاوية على مكونات فعالة مولفة كيميائي اً. ٥ ورغم أن تك وين تلك النيترو ا زمينات أثناء تصنيع معظم الأدوية غير متوقع، فإن إمكانية تلويثها بالتبادل أو احتوائها على الأمينات والنتريتات من دون قصد هي التي دفعت إلى مطالبة الشركات بإج ا رء هذه الاستع ا رضات التحوطية التي يتوقع أن يكون نطاقها واسعاً وأن تدرس جميع نواحي التصنيع العملية، بما فيها تصنيع منتجات المستحض ا رت الصيدلانية النهائية. كما طلبت وكالة الأدوية الأوروبية من حملة ت ا رخيص تسويق تلك المنتجات استكمال هذا الاستع ا رض في غضون ٦ أشهر.
أساليب الاختبار
تشكل المستويات المتدنية من شوائب النيترو ا زمينات الموجودة بالمنتجات تحديات في مجال الاختبار. وتسهيلاً لاختبار العينات، فقد نشرت إدارة الأدوية والأغذية بالولايات المتحدة العديد من أساليب الاختبار التي قد يُنظر فيها عند تقدير ما تحتويه المكونات الفعالة للمستحض ا رت الصيدلانية ومنتجات المستحض ا رت الصيدلانية النهائية من نيترو ا زمينات.
https://www.USFDA.gov/media/124025/download
https://www.USFDA.gov/media/115965/download
https://www.USFDA.gov/media/130801/download
https://www.USFDA.gov/media/131868/download
وأوصت إدارة الأدوية والأغذية بالولايات المتحدة باتباع أسلوب قياس الطيف الكلي العالي الاستبانة لاستش ا رب السوائل عند اختبار ال ا رنيتيدين بسبب ما يهيؤه هذا الأسلوب من ظروف اختبارها في درجات ح ا ررة منخفضة؛ لأن إج ا رء بعض أساليب الاختبار في درجات ح ا ررة مرتفعة قد يسفر عن تكوين العينة لمركبات ثنائي مثيل أمينات النيترو ا زمين. ١٣
وبالمثل، فقد نشرت أيضاً شبكة المختب ا رت الرسمية المعنية بم ا رقبة الأدوية والتابعة لمجلس أوروبا العديد من الأساليب التي قد تُستعمل في اختبار النيتر و ا زمينات، وهي متاحة على عنوان الموقع الإلكتروني التالي:
https://www.edqm.eu/en/ad-hoc-projects-omcl-network
توصيات
فيما يلي خطوات ينبغي أن تتخذها الوكالات التنظيمية فيما يتعلق بالمنتجات الحاوية على مركبات السارتان وال ا رنيتيدين وغيرها من المنتجات التي تُحدّد على أنها حاوية على النيترو ا زمينات، وذلك لتحقيق ما يلي: التحقق من مستويات النيتر و ا زمينات الموجودة بالمنتجات المطروحة في أسواقها، سواء بالاستعانة بالمختب ا رت الوطنية لاختبارها أم بما يصدر من تصريحات ذاتية عن موردي المنتجات أنفسهم، على أن تُستعمل أساليب اختبار مناسبة للتحقق منها. مطالبة حملة ت ا رخيص تسويق تلك المنتجات بإج ا رء تقييمات للمخاطر لتحديد أسباب تلوث المنتجات بالنيترو ا زمينات وتعيين حدود تكفل التحكم في أن تكون مستويات هذه الشوائب فيها دون المستويات المقبولة. مطالبة حملة ت ا رخيص تسويق تلك المنتجات بإدخال تعديلات تكفل انعدام وجود النيتر و ا زمينات في المنتجات أساس اً في المستقبل، مهما كانت مستوياتها.
وبوصف القيم الوارد ذكرها في الجدول ١ من التدابير المؤقتة، فإنها تمثل أفضل المعلومات المتاحة فيما يخص المدخول المسموح به يومياً من تلك الشوائب. أما بالنسبة إلى سائر شوائب النيترو ا زمينات غير المدرجة في هذا الجدول، فإنه يُوصى بتطبيق المبادئ المبينة بإيجاز في المبدأ التوجيهي ICH's M7(R1) 8 لغرض تحديد المدخول المقبول منها.
وبناءً على ما أجري من تحقيقات بشأن وجود النيتروزامينات، فإن من الواضح أن نطاق النظر بالكامل في احتمال تلوث أحد منتجات المستحضرات الصيدلانية النهائية بالنيتروزامينات هو نطاق يجب أن يكون أوسع من إمكانية بحث موضوع استعمال مصادر الأمينات والنيتريتات بالتزامن في إعداد المكونات الفعالة لمنتجات المستحضرات الصيدلانية هذه. ولابد أن تجري شركات تصنيع جميع منتجات المستحضرات الصيدلانية النهائية تقييماً لجميع الظروف التي قد تسفر دون قصد عن تلويث منتجاتها بالنيتروزامينات، وأن تتخذ خطوات تخفف وطأة هذه المخاطر. ويرد وصف مفصل للعوامل التي ينبغي مراعاتها في الطلب الموجه من الاتحاد الأوروبي إلى شركات التصنيع.5
وينبغي في الحالات التي يُلاحظ فيها أن مستوى أحد شوائب النيتروزامينات الموجودة بالمنتجات هو دون الحدود المقبولة مؤقتاً أن يُنظر عموماً إلى تلك المنتجات على أنها مأمونة وأن من الجائز إبقاءها مطروحة في الأسواق.
أمّا في الحالات التي تتجاوز فيها مستويات النيتروزامينات الموجودة بالمنتجات الحدود المقبولة أو يُلاحظ بها وجود أكثر من نيتروزامين واحد، فإنه ينبغي عموماً ألا يُسمح بطرح تلك المنتجات في الأسواق. ولكن يجب أيضاً أن تقوم كل واحدة من السلطات الوطنية، لدى نظرها في اتخاذ هذا الإجراء، بموازنة الآثار التي يخلفها انتفاء المنتج من الأسواق على المريض، الأمر الذي ينطوي على تحديد مدى توفر العلامات التجارية أو العلاجات البديلة في أسواقها والآثار السريرية المترتبة على وقف تناول المريض للعلاج أو تحوله إلى تناول آخر يختلف عنه.
ويُنصح المرضى بجميع الحالات المعروضة حتى الآن بعدم وقف تناولهم لعلاجاتهم ما لم ينصحهم بذلك أحد مهنيي الرعاية الصحية.
وستواصل المنظمة رصد مشكلة تلوث المنتجات بالينيتروزامينات وتقديم أحدث المعلومات عنها، حسب اللزوم. وينبغي أيضاً إيلاء اهتمام للموقعين الإلكترونيين لكل من إدارة الأدوية والأغذية بالولايات المتحدة ووكالة الأدوية الأوروبية، اللذين سيُنشر فيهما ما يستجد عن التحقيقات الجارية من معلومات.
المراجع
2 - https://www.ema.europa.eu/en/news/ema-review-ranitidine-medicines-following-detection-ndma
5 - https://www.ema.europa.eu/en/news/ema-advises-companies-steps-take-avoid-nitrosamines-human-medicines
6 - February 2019, EMA/44960/2019: Sartan medicines: companies to review manufacturing processes to avoid
presence of nitrosamine impurities.
9 - 20 August 2019 EMA/351053/2019 rev 1: Temporary interim limits for NMBA, DIPNA and EIPNA impurities in
sartan blood pressure medicines.
8 - https://database.ich.org/sites/default/files/M7_R1_Guideline.pdf
11 - https://www.ema.europa.eu/en/medicines/human/referrals/ranitidine-containing-medicinal-products
12 - https://www.USFDA.gov/drugs/drug-safety-and-availability/laboratory-tests-ranitidine.
WHO Global Surveillance and Monitoring System
for Substandard and Falsified Medical Products
For further information, please visit: http://www.who.int/medicines/regulation/ssffc/en/