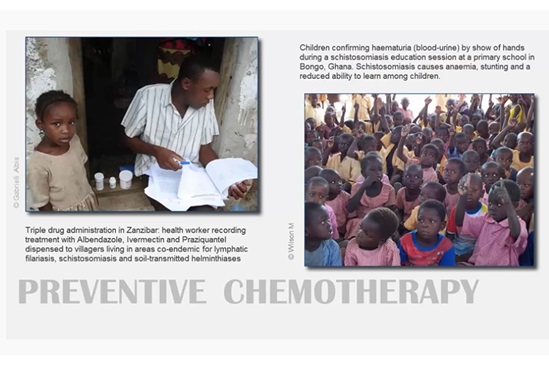
Le paquet de formulaires intégrés pour la CP - Planification, demande de médicaments et rapports
Mise en œuvre de la chimiothérapie préventive intégrée
La sélection des médicaments anthelminthiques recommandés par l'OMS pour une utilisation dans les programmes de santé publique est conçu pour contrôler et éliminer les helminthiases. Beaucoup de ces médicaments sont à large spectre, permettant de traiter plusieurs maladies simultanément. Les interventions préventives de chimiothérapie (CP) devraient donc être fondées sur l'utilisation optimale et coordonnée des médicaments disponibles plutôt que de cibler des helminthiases spécifiques. Où opérationnellement faisable et épidémiologiquement justifié, l'OMS recommande la mise en œuvre intégrée et coordonnée des combinaisons de médicaments vermifuges pour cibler de multiples maladies.
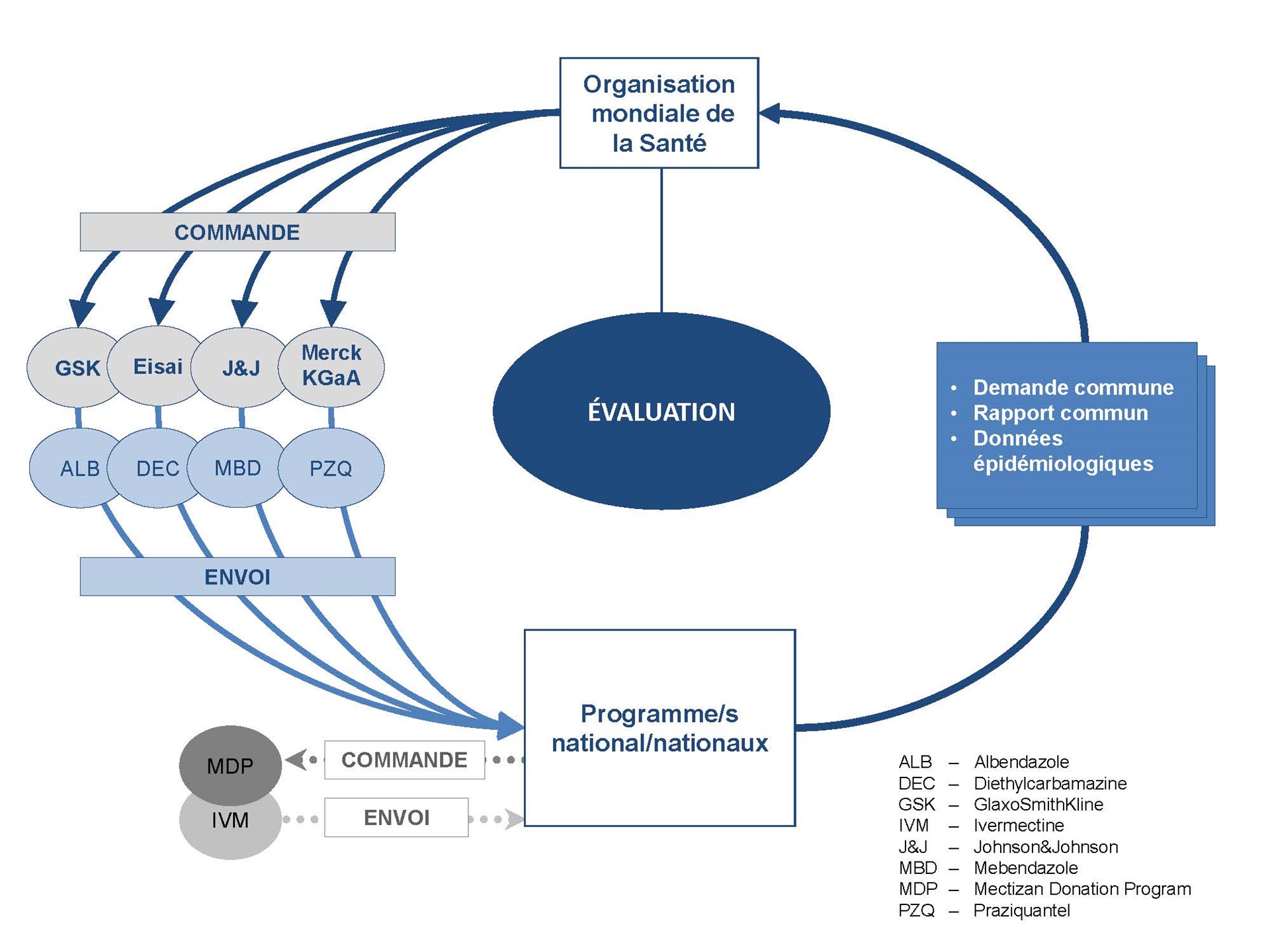
Mécanisme et outils pour soutenir la mise en œuvre intégrée de la chimioprévention
Dans le cadre des efforts mondiaux visant à accélérer l'expansion de la chimioprévention pour l'élimination et le contrôle de la filariose lymphatique (FL), la schistosomiase (SCH) et les géohelminthiases (STH), l'OMS facilite l'approvisionnement des médicaments suivants, offerts par l'industrie pharmaceutique : diethylcarbamazine, albendazole, mébendazole et praziquantel. L'OMS contribue également à fournir de l'ivermectine pour l'onchocercose (ONCHO) et les programmes d'élimination de la filariose lymphatique.
Un mécanisme commun et un ensemble de formulaires ont été conçus pour faciliter le processus de demande de médicaments, d'examen et de rapports ainsi que pour améliorer la coordination et l'intégration des activités entre les différents programmes.
- Formulaire de demande commune de médicaments pour la chimioprévention (FDCM) – conçue pour aider les pays à quantifier le nombre de comprimés de médicaments pertinents nécessaires pour atteindre la population cible prévue et les districts d'une manière coordonnée et intégrée contre plusieurs maladies au cours de l'année pour laquelle les médicaments sont demandés.
- Formulaire de rapport commun (FRC) – conçu pour aider les pays à rendre compte des progrès annuel sur la distribution intégrée et coordonnée des médicaments pour diverses maladies, dans l'année de référence, dans un format standardisé.
- Formulaire de déclaration des données épidémiologiques (FDDE) – ce formulaire est conçu pour standardiser les rapports de données épidémiologiques, au niveau national, sur la filariose lymphatique, l'onchocercose, les géohelminthiases et la schistosomiase. Les autorités nationales sont invitées à remplir ce formulaire et à le soumettre à l'OMS, sur une base annuelle, joint au formulaire de rapport commun (FRC).
Tous les demandes sont soumis à un examen et/ou à la disponibilité des médicaments. En outre, l'utilisation de médicaments donnés doit être dûment signalée à l'OMS à la fin des activités de traitement.
Soumission du paquet de formulaires intégrés pour la CP
Les rapports générés dans le FDCM et dans le FRC (feuilles de calcul SUMMARY) doivent être imprimés et signés par le coordinateur MTN ou un représentant du ministère de la santé afin d'approuver officiellement la demande du pays pour ces médicaments et les progrès annuels rapportés du ou des programmes nationaux. La date de la signature doit également être indiquée. Une fois les signatures obtenues, les copies scannées des feuilles de calcul du SUMMARY, ainsi que les versions Excel complètes du FDCM, du FRC et du FDDE peuvent être soumises à l'OMS.
Notez que tous les formulaires doivent être soumis au représentant de l'OMS du bureau de pays de l'OMS concerné avec des copies électroniques à PC_JointForms@who.int et au point focal régional MTN concerné. La date limite de soumission du paquet de formulaires intégré (JAP) dépend de la date de mise en œuvre prévue, comme suit :
- Pendant l'année de mise en œuvre, le FRC peut être préparé et partiellement complété après chaque cycle d'administration massive de médicaments (AMM), lorsque les données de traitement deviennent disponibles. Le rapport final doit être soumis dans les 3 mois suivant la mise en œuvre du dernier cycle et au plus tard le 31 mars de l'année de mise en œuvre suivante.
- Pour garantir la livraison des médicaments à temps, la demande de médicaments CP doit être soumise au moins 9 mois avant la première date d'administration massive de médicaments prévue dans l'année civile de la demande. Par exemple, si un pays prévoit de mener deux cycles AMM en mai et octobre 2023, la demande doit être soumise avant août 2022. Ce délai est nécessaire pour examiner et approuver la demande, passer les commandes, fabriquer les médicaments CP et les expédier au pays. Certains pays qui ont des procédures spécifiques nécessitant plus de temps doivent présenter leur demande plus tôt, en tenant compte du temps supplémentaire requis, par exemple, l'inspection avant expédition.
- Le FDDE fait partie du JAP et doit être soumis annuellement avec les autres formulaires. Si aucune enquête épidémiologique n'a été menée pendant l'année considérée, le formulaire soumis doit rester vierge.
Le paquet de formulaires intégrés pour la CP, et en particulier le FDCM, ne sera pas approuvé sans la soumission de la version finale du FRC. Si la CP n'a pas été mise en œuvre comme prévu pendant l'année de mise en œuvre, le FRC doit être soumis avec des données complètes fournies dans COUNTRY_INFO et une explication écrite des raisons dans la case d'informations supplémentaires de la feuille de calcul SUMMARY.
Collecte et rapport des données aux niveaux des communautés et des districts
L'enregistrement et la collecte d'informations fiables sur l'utilisation des médicaments (cf. couverture des médicaments) aux niveaux périphériques et de district et la compilation de ces informations au niveau national est essentielle pour la complétion du Formulaire de rapport commun (FRC).
Matériel d'entraînement